Le virus Andes tue entre 35 et 40 % de ses victimes. Entre l'exposition et les premiers signes respiratoires, il s'écoule en moyenne 4 à 14 jours — une fenêtre silencieuse pendant laquelle le virus prolifère sans symptôme visible. Puis, en l'espace de 48 à 72 heures, un adulte jusque-là en bonne santé bascule vers une détresse respiratoire aiguë mettant sa vie en danger. Chaque heure compte. Chaque signe compte.
Le syndrome cardiopulmonaire à hantavirus (SCPH), appelé HPS en anglais (Hantavirus Pulmonary Syndrome), est l'une des infections virales les plus rapidement évolutives connues en médecine d'urgence. Sa progression suit un schéma en plusieurs phases distinctes, chacune avec ses propres marqueurs cliniques, ses pièges diagnostiques et ses seuils d'alerte. Comprendre cette cinétique, c'est comprendre pourquoi un retard de quelques heures dans la prise en charge peut être fatal.
Cet article détaille, phase par phase, l'évolution clinique de l'infection à hantavirus chez un patient développant un SCPH — de l'incubation silencieuse à la phase cardiopulmonaire critique, en passant par les marqueurs biologiques qui permettent d'anticiper la dégradation avant qu'elle ne survienne.
Phase 0 : L'incubation silencieuse (4 à 42 jours)
La première phase de l'infection à hantavirus n'est pas clinique — elle est biologique. Le virus, inhalé par des aérosols de déjections de rongeurs infectés, pénètre dans l'organisme par les voies respiratoires et commence à se répliquer dans les cellules endothéliales des capillaires pulmonaires. Aucun symptôme n'est encore perceptible. Le patient se sent bien. C'est précisément ce qui rend cette phase dangereuse.
Durée d'incubation selon les espèces virales :
- Virus Andes (Amérique du Sud) : 4 à 42 jours — la fourchette la plus large, justifiant une surveillance prolongée après exposition
- Virus Sin Nombre (Amérique du Nord) : 1 à 6 semaines en moyenne
- Hantavirus européens (Puumala, Dobrava) : 2 à 4 semaines pour le syndrome hémorragique rénal (différent du SCPH)
La durée médiane d'incubation pour le virus Andes — responsable des cas récents documentés en Europe dont l'épidémie liée au navire MV Hondius en 2024 — est estimée entre 2 et 3 semaines. Sur les 22 contacts exposés lors de cet événement, 3 sont décédés, confirmant un taux de létalité compatible avec les données historiques.
Ce qui se passe dans l'organisme pendant l'incubation :
- Le virus se fixe sur les intégrines des cellules endothéliales pulmonaires
- Réplication virale initiale dans les poumons et les ganglions lymphatiques régionaux
- Dissémination systémique par virémie (passage dans le sang)
- Activation progressive de la réponse immunitaire innée
- Début de la perméabilité capillaire — encore subclinique à ce stade
Implication pratique : Toute personne ayant été en contact avec des rongeurs dans une zone d'endémie (ou en provenance d'une zone endémique) doit être surveillée pendant au moins 6 semaines après l'exposition potentielle. L'absence de symptômes au cours des 2 premières semaines ne constitue pas une confirmation d'absence d'infection.
Phase 1 : Le prodrome trompeur (jours 1 à 5 après les premiers symptômes)
Lorsque les premiers symptômes apparaissent, ils sont systématiquement non spécifiques. C'est le principal piège diagnostique de l'infection à hantavirus : la phase prodromique ressemble à une grippe banale, à un syndrome viral estival, à une gastro-entérite. Aucun signe respiratoire n'est présent à ce stade. C'est là que le diagnostic est le plus souvent manqué.
Symptômes cardinaux de la phase prodromique :
- Fièvre élevée, typiquement entre 38 °C et 40 °C, d'apparition brutale
- Céphalées intenses, souvent frontales et rétro-orbitaires, résistantes aux antalgiques usuels
- Myalgies sévères prédominant dans le dos, les cuisses et les épaules — signe d'orientation important
- Asthénie profonde et fatigue marquée, disproportionnée par rapport à la durée d'évolution
- Nausées et vomissements, présents dans 60 à 70 % des cas selon les séries CDC
- Douleurs abdominales, parfois au premier plan, pouvant orienter à tort vers une pathologie digestive
- Frissons et sueurs nocturnes
Absents à ce stade (et leur absence est diagnostiquement significative) :
- Toux — son apparition signe l'entrée dans la phase de transition
- Dyspnée — absente pendant les 4 à 5 premiers jours
- Signes respiratoires auscultatoires — poumons cliniquement normaux
- Éruption cutanée — non caractéristique de l'infection à hantavirus
Scénario clinique réel : Considérons un homme de 34 ans, randonneur, qui revient d'un séjour de 3 semaines en Argentine dans la région des Andes. Au 18e jour après son retour, il consulte son médecin traitant pour "syndrome grippal" : fièvre à 39,2 °C, courbatures intenses dans les jambes, maux de tête depuis 48 heures, sans toux. Le médecin prescrit du paracétamol et un arrêt de travail. Le patient rentre chez lui. 36 heures plus tard, il sera admis aux urgences en détresse respiratoire.
Ce scénario n'est pas hypothétique — il correspond aux profils décrits dans les rapports épidémiologiques du CDC et de l'ECDC. La fenêtre diagnostique existait dès la phase prodromique. Elle n'a pas été saisie.
Marqueurs biologiques pendant la phase prodromique :
- Thrombocytopénie débutante (baisse des plaquettes) — signal précoce mais souvent ignoré
- Hématocrite normal ou légèrement élevé (hémoconcentration initiale)
- Leucocytes normaux ou légèrement augmentés
- Absence de syndrome inflammatoire majeur en début de phase
- Radiographie thoracique : normale dans la majorité des cas à J1-J3
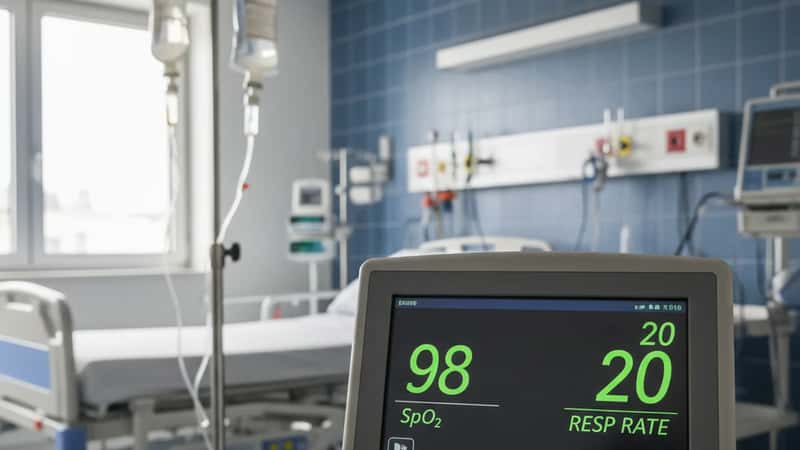
Phase 2 : La transition critique (jours 4 à 6 — fenêtre d'alerte)
La phase de transition est courte — 24 à 48 heures — mais elle représente la dernière fenêtre d'intervention avant la dégradation cardiopulmonaire. C'est ici que la reconnaissance précoce des signes d'alerte peut faire la différence entre une prise en charge en soins intensifs à temps et une admission trop tardive.
Signes cliniques de la transition :
- Apparition d'une toux sèche non productive — premier signal respiratoire
- Polypnée débutante (fréquence respiratoire > 20/min au repos)
- Persistance ou aggravation de la fièvre malgré les antipyrétiques
- Sensation de "pression thoracique" ou d'essoufflement à l'effort léger
- Aggravation brutale de l'état général après une relative stabilité de 3-4 jours
- Anxiété inexpliquée — liée à l'hypoxémie débutante
Marqueurs biologiques d'alerte (à surveiller activement à ce stade) :
- Thrombocytopénie franche (plaquettes < 100 000/mm³) — signe de gravité
- Hémoconcentration marquée : hématocrite > 50 % ou hémoglobine très élevée
- Leucocytose avec myélémie (présence de cellules immatures dans le sang) — marqueur quasi pathognomonique
- Lymphocytes immunoblastiques sur le frottis sanguin
- Élévation des LDH — reflet de la lésion tissulaire
- Radiographie thoracique : infiltrats bilatéraux débutants, parfois discrets
Ce que fait le virus à ce stade : Le hantavirus compromet la barrière endothéliale des capillaires pulmonaires. La perméabilité vasculaire augmente. Un liquide plasmatique commence à s'accumuler dans les espaces interstitiels puis alvéolaires des poumons — c'est l'œdème pulmonaire cardiogénique qui s'installe. Simultanément, la contractilité myocardique diminue, précipitant le tableau de choc cardiogénique qui caractérise la phase suivante.
Décision clinique à ce stade : Devant une combinaison de fièvre + myalgies + thrombocytopénie + exposition potentielle à des rongeurs dans une zone endémique, l'admission en milieu hospitalier avec surveillance rapprochée s'impose. Ne pas attendre la confirmation sérologique pour agir.
Phase 3 : La crise cardiopulmonaire (jours 5 à 10 — mortalité 35-40 %)
C'est la phase qui tue. Le syndrome cardiopulmonaire à hantavirus atteint sa pleine expression clinique entre le 5e et le 10e jour après l'apparition des symptômes. La dégradation peut être foudroyante : certains patients passent d'une légère dyspnée à une insuffisance respiratoire aiguë nécessitant une intubation en moins de 12 heures.
Tableau clinique complet de la phase cardiopulmonaire :
- Détresse respiratoire aiguë (SDRA) : SpO₂ < 90 % malgré l'oxygène, fréquence respiratoire > 30/min, utilisation des muscles accessoires
- Œdème pulmonaire non cardiogénique (ou mixte) : crépitants bilatéraux à l'auscultation, expectoration mousseuse rosée dans les cas sévères
- Choc cardiogénique : hypotension artérielle < 90/60 mmHg, extrémités froides, marbrures
- Tachycardie sinusale persistante > 120/min, parfois arythmies
- Cyanose centrale
- Oligurie et insuffisance rénale aiguë associée dans 30 à 50 % des cas
Imagerie et biologie à ce stade :
- Radiographie thoracique : opacités alvéolaires bilatérales diffuses, aspect "en ailes de papillon"
- Scanner thoracique : consolidations alvéolaires, verre dépoli diffus, épanchements pleuraux bilatéraux
- Échocardiographie : fraction d'éjection ventriculaire gauche effondrée (< 45 %), parfois < 20 % dans les formes sévères
- Biologiquement : thrombocytopénie < 50 000/mm³, hématocrite > 55-60 %, LDH très élevées, troponine positive (atteinte myocardique)
- Gaz du sang : hypoxémie sévère (PaO₂/FiO₂ < 200), acidose métabolique
Pourquoi 35 à 40 % des patients meurent-ils ? L'ECDC et le CDC documentent ce taux de mortalité de façon consistante depuis les années 1990. La physiopathologie explique cette létalité : contrairement à d'autres virus respiratoires, le hantavirus provoque une défaillance cardiopulmonaire combinée. Les poumons s'inondent pendant que le cœur ne peut plus assurer le débit nécessaire aux organes vitaux. Cette double défaillance, survenant simultanément et rapidement, dépasse fréquemment les capacités de compensation physiologique du patient.
Ce qui fait la différence entre survivre et mourir :
- Délai d'admission en réanimation : les patients admis avant l'installation du choc complet ont un pronostic significativement meilleur
- Disponibilité de l'ECMO (oxygénation par membrane extracorporelle) dans l'établissement d'accueil
- Expertise de l'équipe de réanimation dans la gestion du SDRA
- Comorbidités : immunodépression, obésité et pathologies cardiovasculaires aggravent le pronostic
- Charge virale initiale et réponse immunitaire individuelle — facteurs encore en cours d'étude
Suite du scénario clinique : Le randonneur de 34 ans est arrivé aux urgences avec une SpO₂ à 82 % sous air ambiant. Intubé en 20 minutes, transféré en réanimation. L'échocardiographie montre une fraction d'éjection à 18 %. L'équipe place une ECMO veino-artérielle. Après 9 jours de réanimation intensive, il est sevré de l'ECMO, extubé au 14e jour. Il sortira de l'hôpital sans séquelle pulmonaire majeure. Il fait partie des 60 à 65 % de patients qui survivent — grâce à une prise en charge immédiate dans un centre de référence.
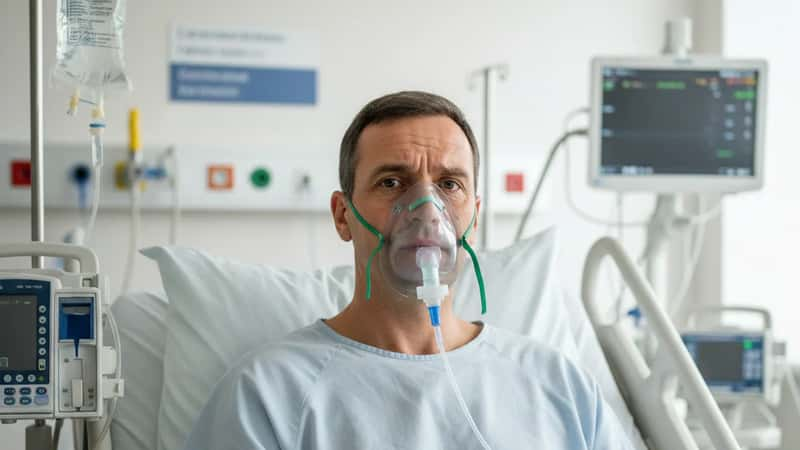
Phase 4 : La diurèse et la récupération (jours 10 à 21)
Les patients qui survivent à la phase cardiopulmonaire entrent généralement dans une phase de récupération dont le premier signe est une augmentation marquée de la diurèse — le corps élimine le liquide qui avait envahi les poumons. C'est un signe clinique de bon pronostic.
Marqueurs de récupération :
- Polyurie abondante (> 2 à 3 litres/24h) — signe de levée de la perméabilité capillaire
- Amélioration progressive des paramètres respiratoires, réduction des besoins en oxygène
- Remontée des plaquettes après le nadir
- Normalisation progressive de l'hématocrite
- Amélioration de la fraction d'éjection ventriculaire à l'échocardiographie de contrôle
- Régression des opacités pulmonaires en imagerie (délai : 1 à 3 semaines)
Séquelles potentielles à long terme :
- Fatigue persistante pendant 3 à 6 mois après la guérison — signalée par la majorité des survivants
- Légère diminution de la capacité d'effort dans les 6 premiers mois
- Troubles anxieux et syndrome de stress post-traumatique liés à l'expérience de réanimation
- Dans de rares cas : insuffisance rénale résiduelle légère
Une particularité importante : contrairement aux infections à hantavirus européens causant un syndrome hémorragique avec atteinte rénale (Hantavirus Fever with Renal Syndrome ou FHSR, causé notamment par le virus Puumala en France), le SCPH causé par le virus Andes ou Sin Nombre ne laisse généralement pas de séquelle rénale permanente chez les survivants.
Le diagnostic : comment confirmer l'infection à hantavirus
La confirmation diagnostique repose sur des analyses biologiques spécialisées, disponibles en France via le Centre National de Référence (CNR) des Hantavirus, rattaché au CHU de Strasbourg.
Méthodes diagnostiques disponibles :
Sérologie IgM/IgG par ELISA : méthode de référence en phase aiguë. Les IgM sont détectables dès J1-J3 des symptômes et persistent plusieurs semaines. Les IgG apparaissent plus tardivement et persistent des années. Un titre élevé d'IgM spécifiques en contexte clinique compatible suffit au diagnostic de présomption.
RT-PCR (reverse transcription polymerase chain reaction) : détection du génome viral dans le sang ou les tissus. Très sensible en phase virémique (J1-J5), la sensibilité diminue ensuite. Permet l'identification précise de l'espèce virale et la phylogénie des souches.
Immunohistochimie : utilisée post-mortem ou sur biopsies, permet de visualiser l'antigène viral dans les tissus infectés — poumons, reins, rate.
Culture virale : réservée aux laboratoires de haute sécurité (BSL-4), non disponible en routine clinique.
Délais diagnostiques pratiques :
- Sérologie ELISA : résultat en 24 à 48 heures en urgence
- RT-PCR : 6 à 12 heures dans les centres équipés
- Le diagnostic de présomption clinique (sans attendre la biologie) doit guider la prise en charge en urgence
En France métropolitaine, la détection d'un cas suspect de SCPH (hantavirus non européen, avec exposition à risque identifiée) impose une notification immédiate à Santé publique France et au CNR. L'alerte précoce permet l'enquête épidémiologique et la recherche de cas contacts.
Les signes d'alerte absolus : quand appeler le 15
Face à un patient présentant un contexte épidémiologique compatible (voyage récent en Amérique du Sud ou du Nord, contact avec des rongeurs, activité en milieu rural), les signes suivants justifient un appel immédiat au SAMU (15) ou une orientation vers les urgences sans délai :
Signes d'urgence absolue :
- Dyspnée au repos ou à l'effort minime, quelle que soit la saturation affichée
- Fréquence respiratoire > 22/min au repos
- SpO₂ < 95 % sous air ambiant
- Hypotension artérielle (tension systolique < 100 mmHg)
- Confusion, agitation, somnolence inexpliquée
- Douleur thoracique associée à la fièvre
- Cyanose des lèvres ou des extrémités
Signes biologiques imposant l'hospitalisation immédiate :
- Plaquettes < 100 000/mm³ en contexte fébrile + exposition à risque
- Hémoconcentration (hématocrite > 50 %)
- Leucocytose avec déviation gauche et myélémie
- Infiltrats pulmonaires bilatéraux à la radiographie
Le message central est celui-ci : dans une infection à hantavirus de type SCPH, l'état clinique peut se détériorer de façon catastrophique en quelques heures. La fenêtre entre "patient fébrile qui se plaint de courbatures" et "patient intubé en réanimation" peut se fermer en moins de 24 heures. Aucun signe d'alerte ne doit être banalisé.
Avertissement médical (YMYL) : Cet article est rédigé à des fins d'information médicale générale et ne se substitue en aucun cas à un avis médical professionnel, à un diagnostic ou à un traitement. Les informations présentées sont basées sur des données épidémiologiques et cliniques issues de l'ECDC, du CDC, de l'OMS et de Santé publique France, à jour au moment de la rédaction. Toute suspicion d'infection à hantavirus constitue une urgence médicale. Appelez le 15 (SAMU) immédiatement. Ne vous fiez pas à cet article pour prendre des décisions médicales individuelles.










